醫療器材單一識別技術使醫療 ID 和條碼的讀取自動化
資料提供者:DigiKey 北美編輯群
2023-10-26
2013 年,美國食品藥物管理局 (FDA) 實施醫療器材單一識別系統,又稱為 UDI 規範。此規範要求在製造、經銷和使用醫療器材時採用現代化文件編制,以一致的方式追蹤及識別醫療器材,進而提高病患的安全性。美國 UDI 規範近似於歐洲的醫療器材法規要求,或其他國家的類似法規,不僅提高報告的準確度,還能在產品被召回或發生不良事件時,簡化分析作業。
2023 年 9 月 24 日起,FDA 將全面針對醫療器材標籤與包裝強制執行國家健康相關產品代碼和藥物代碼編號。該日之後貼標的任何醫療產品,必須完全遵守 UDI 命令。這項命令將影響以下產品:
- Class 3 性命攸關型產品,如心律調節器和人工植體
- Class 2 中度關鍵產品,如注射器、導管和可吸收縫線
- Class 1 低風險產品,如牙線、醫用長袍和氧氣面罩
全面強制執行此命令後,若醫療裝置沒有可掃描的條碼,即使有人員可讀的標籤,且即使多數使用者通常認為能夠輕鬆識別該產品,該醫療器材也不再被視為有效/可用的產品。全面執行這項命令,將促使醫療業和醫療保險帳單領域全面跟進。
 圖 1:某些手持式直接零件標記 (DPM) 條碼驗證器,具有先進的照明及其他軟體,能自動找出符號並循環執行所有設定值,在讀取特定的 DPM 標記和現有的材料基板時能達到最佳效果。事實上,圖中的 LVS-9585 對 DPM 零件和印刷標籤都能驗證,產生完整的分析與報告內容。(圖片來源:Omron Automation)
圖 1:某些手持式直接零件標記 (DPM) 條碼驗證器,具有先進的照明及其他軟體,能自動找出符號並循環執行所有設定值,在讀取特定的 DPM 標記和現有的材料基板時能達到最佳效果。事實上,圖中的 LVS-9585 對 DPM 零件和印刷標籤都能驗證,產生完整的分析與報告內容。(圖片來源:Omron Automation)
由立約實體 (品牌持有人) 負責
在美國,UDI 代碼的準確度和品質,由各醫療產品的 IP 擁有者和使用者端的品牌自行負責。這點特別重要,因為醫療產品市場大多是根據合約委託製造,並且外包給其他組織的廠房。因此,立約組織有責任確保整條供應鏈符合 UDI,且生產的標籤準確無誤。
醫療器材單一識別技術的起源
UDI 是靜態的醫療器材識別碼。但當包裝內的產品數量有變,可能需要使用其他新的識別碼。核發機構規定了這些細節的辨別方法。同樣地,在醫療器材包裝的無菌狀況改變時,醫療器材識別碼也可能變更。改變醫療器材的目標市場時 (醫療器材販售國),醫療器材識別碼也可能因標籤語言或 CE 標誌而需要更改。
在實施 UDI 規範之前,醫療器材製造商可能已為產品標示特定的零件編號。經銷商會更改此零件編號,醫療照護提供者或醫院之後還會再改一次。由於醫療器材到達患者環節之前每個實體都可能變更過零件編號,因此幾乎不可能追蹤產品、處理召回事件、防止偽造,或準確有效率地訂購新的庫存。
相關內容:實作穩健的可追溯性解決方案
目前,每個醫療器材都被指派標準化的永久識別碼 (UDI),讓所有實體能更快速精準地識別醫療器材,最終減少醫療錯誤。此 UDI 是一種英數代碼,含有兩個關鍵的資料:
- 醫療器材識別碼
- 生產識別碼
醫療器材識別碼是醫療器材被指派的一種靜態標籤,當中列出貼標者 (通常是醫療器材製造商),以及醫療器材的型號。相較之下,生產識別碼中的資料可能不一,可納入的資料中很多也是選擇性納入。這些資料可能包括小批次代碼、組批代碼、序號、到期日和製造日期。簡單地說,凡製造商或貼標者認為必須納入以便支援醫療器材追蹤,就能選擇納入該資料。
每個 UDI 標籤必須以兩種形式呈現此資訊:
- 人員可讀形式 (純文字)
- 機器可讀形式 (可利用條碼或 RFID 讀取器讀取)
只要是能滿足多種醫療應用的醫療器材,必須將 UDI 直接標於醫療器材上,而非包裝上。此規範亦適用於能多次使用的醫療器材。
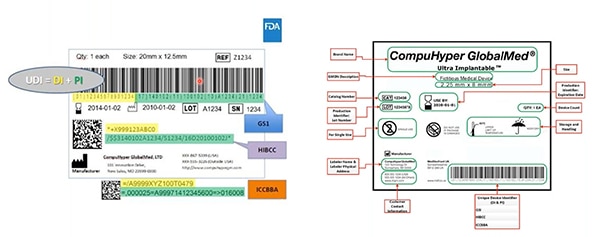 圖 2:UDI 核發機構 GS1、HIBCC 和 ICCBBA 建立 UDI 識別碼;指派 UDI 允許的符號系統;定義哪些技術可以用於 UDI;以及指定所需的 UDI 標記品質。此樣本中螢光黃底色是醫療器材識別碼;螢光綠底色是生產識別碼。其他元素包括人員可讀資訊,這些元素也編碼到機器可讀條碼中。(圖片來源:FDA)
圖 2:UDI 核發機構 GS1、HIBCC 和 ICCBBA 建立 UDI 識別碼;指派 UDI 允許的符號系統;定義哪些技術可以用於 UDI;以及指定所需的 UDI 標記品質。此樣本中螢光黃底色是醫療器材識別碼;螢光綠底色是生產識別碼。其他元素包括人員可讀資訊,這些元素也編碼到機器可讀條碼中。(圖片來源:FDA)
所有醫療器材必須在全球 UDI 資料庫中註冊,以便在召回時追蹤醫療器材以及方便公眾存取醫療器材的資訊。經 FDA 認可的核發機構有權建立唯一識別碼,供醫療器材製造商放置於產品上。
相關白皮書:Staying Current on Traceability (可追溯性最新發展)
UDI 掃描技術與技巧
從製造到使用,UDI 標籤能以幾種方式驗證。
線上驗證是由大型機械內建的技術執行,以便在生產時快速準確地處理大量產品。在先進軟體的支援下,這些技術偶爾採工業級標籤印表機的形式。這些印表機能自行進行線上驗證,確認標籤生產作業一建立 UDI 資訊時,立刻就能依照嚴格的產業標準讀取該資訊。例如,Omron Automation V275 驗證器係搭配 Zebra 熱敏印刷機使用,以遵守 ISO 15426 和核發機構 GS1 的 FDA 合規性標準。
相關內容:Omron Traceability Solutions (Omron 可追溯性解決方案)
在其他地點,線上驗證的形式為自動化生產線專用的機械視覺側面輸送機,結合條碼讀取能力,能在高速生產線上,十分快速準確地驗證高混合性產品的 UDI 標示。Omron Automation 的 MicroHAWK 產品在這方面表現優異,具備先進的感測器,並搭配小型化結構和許多連線選擇,包括 Ethernet/IP 和 PROFINET。
相關內容:Avoid the Liability of Mislabeling (避免因貼錯標籤身陷法律責任)
相較之下,標籤批次採樣最適合使用離線 UDI 驗證方式,以確保品質。離線驗證經常在醫療器材送離或送達場所時用於樣品測試,能為經銷鏈上游的線上驗證系統提供補強作用。
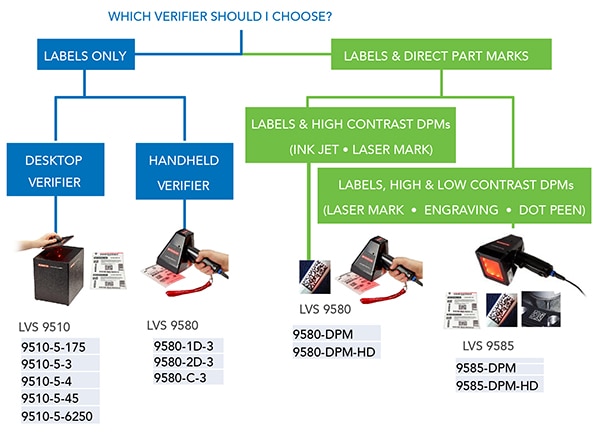 圖 3:比起印於黏貼式標籤上的 UDI,直接標示於產品上的 UDI 需使用不同的驗證器。(圖片來源:Omron Automation)
圖 3:比起印於黏貼式標籤上的 UDI,直接標示於產品上的 UDI 需使用不同的驗證器。(圖片來源:Omron Automation)
事實上,使用符合 ISO 標準的驗證器,對所有醫療經銷與保健作業都有幫助。考慮使用 Omron 的 LVS 95XX 系列離線式 UDI 驗證產品。使用場所如下:
- 建立代碼的雷射標示站與標籤印表機
- 將代碼套用至產品的場所 (該場所可能與代碼建立區分開或合併)
- 確認範本、格式及其他代碼元素的品管站
指定離線 UDI 驗證器款式
挑選應用最適合的離線 UDI 驗證器,取決於幾個參數。
條碼大小:大型條碼通常比較容易掃描,因為識別碼的視野較大,視野是由鏡頭焦距和感測器的大小定義。考量 Omron Automation 的 LVS-9510 桌上型 UDI 識別碼。此系列產品能讀取線性標籤和 2D 標籤。五個版本具有不同的視野,因此設計人員能根據需驗證的條碼大小,選擇相容的版本。具有拼接特點,能對超出視野的條碼進行分級。
此外,所有 LVS-9510 能自動判定需要何種符號系統和孔徑,以便評估代碼,以及識別和突顯問題點。
 圖 4:使用能驗證線性 (1D) 和二維 (2D) 條碼的設備,能更輕易進行符合 ISO 標準的條碼驗證作業。這種設備有些能判定需要何種符號系統和孔徑,以便評估代碼,以及識別和突顯問題點。圖中的 LVS-9510 具有拼接特點,能對超出視野的條碼進行分級。(圖片來源:Omron Automation)
圖 4:使用能驗證線性 (1D) 和二維 (2D) 條碼的設備,能更輕易進行符合 ISO 標準的條碼驗證作業。這種設備有些能判定需要何種符號系統和孔徑,以便評估代碼,以及識別和突顯問題點。圖中的 LVS-9510 具有拼接特點,能對超出視野的條碼進行分級。(圖片來源:Omron Automation)
條碼類型:掃描器必須讀取核發機構分配的條碼格式,核發機構即 HIBCC、ICCBBA 或 GS1 (2023 年起最常見的核發機構)。GS1 決定了 UPC、線性條碼和 2D 資料矩陣條碼的大小、格式及解析度。
UDI 標記位置:關於醫療器材的直接零件標記 (DPM),這些標記可能非常小,尤其是當用於識別手術儀器和植入式醫療器材時。為了讀取和驗證這種 DPM UDI,Omron 的 LVS-9580 和 LVS-9585 超高密度手持式驗證器具備專用鏡頭,能對各種 DPM 進行分級,包括單元尺寸小至 0.002 英吋的 DPM。LVS-9580 和 LVS-9585 內建的工業級鏡頭,能確保持續準確讀取。最精密的是掃描器內的照明技術,這些技術具有高控制性與高校正能力。除了多個視野外,照明功能還能讓擷取的 UDI 影像立即最佳化。這點特別重要,因為代碼標準不允許事後校正或影像處理。
細談 UDI 掃描器軟體
為了達到最大的效果,用於支援驗證器硬體的 UDI 軟體,必須以直覺的格式呈現診斷資訊。此軟體必須根據 ISO 定義的參數對 UDI 代碼進行分級 (最重要的目的是確認可讀性),而且理想情況下,應針對一系列 UDI 掃描作業追蹤正在惡化的問題。
Omron 每一個 UDI 掃描硬體,都隨附所有必要的軟體。軟體會定期更新,以跟上快速發展的法規和新的業界立法。
Omron 掃描器軟體的主要功能是處理代碼語法。簡單地說,每個條碼或 2D 代碼必須準確擷取所有相關資訊,包括產品類型、批號、數量 (若適用)、到期日、出貨資訊等等。產生的資料字串必須設定為特定格式,以便跟上不斷變化的規定、方法論及醫療產品目的地相關要求。
掃描器製造廠定期更新軟體,能確保即使發佈新的代碼,最終使用者也能跟上腳步。
結論
美國軍方曾希望全面採用類似醫療產業 UDI 系統的 UID 產品追蹤系統,用以減少軍事設施因遺失、重複和未盤點的補給品而造成的大量浪費。這些補給品包括整套 Raytheon 武器,甚至是小型配備針對某些專門用途提供的控制板。今日,UID 的使用層級不一。
UDI 命令卻不會如此。
推動採用 UDI 的口號很簡單:標籤即產品。畢竟,標籤不正確可能會引發一連串事件,浪費醫護人員的時間,並導致醫療器材被丟棄。因此,UDI 必須出現在所有包裝層級上,例如器材、包裝、捆包、外殼和貨板本身。採用滅菌密封的無菌醫療器材,不能為了驗證其類型而破壞密封,因此醫療器材上特別需使用 UDI。
隨著 FDA 要求自 2023 年 9 月 24 日全面遵循 UDI 指令,用於驗證醫療產品的先進掃描技術,將對自動化製造商扮演重大角色,對其服務的機器製造商及最終使用者也是如此。
這種掃描器能滿足十分特殊的 FDA UDI 要求,以確認各種實驗室、醫療與臨床診斷設備上的標籤。離線條碼驗證器能最大程度提升可追溯性、內嵌式機械視覺和先進的 DPM 讀取器的能力。

聲明:各作者及/或論壇參與者於本網站所發表之意見、理念和觀點,概不反映 DigiKey 的意見、理念和觀點,亦非 DigiKey 的正式原則。






